Chapitre 3 − Transformations
1. Le modèle particulaire
- Molécule
- Les molécules sont de petites particules de matière, invisible à l’œil nu. Toute la matière est constituée de molécule (les objets, les gaz, les êtres vivants, …)
Dans le modèle particulaire, on représentera les molécules par un symbole.
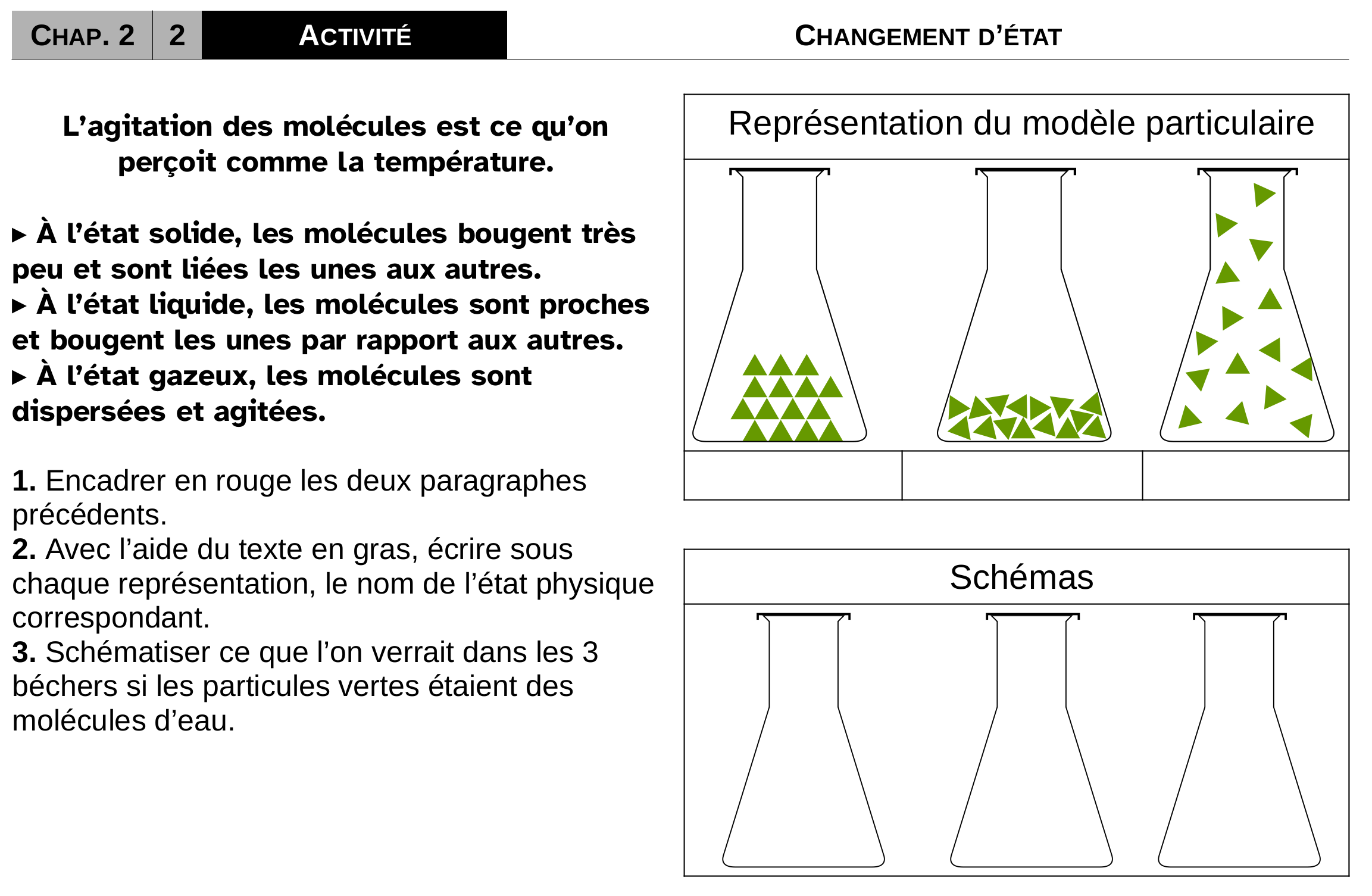
activité p28 question 2
2. L’agitation thermique
En 1827, l’écossais Robert BROWN observe à l’intérieur de grains de pollens, de minuscules particules…
assets/4_pollen.mp4
En 1905, Einstein comprend que ce mouvement est du aux mouvements d’autres particules beaucoup plus petite et beaucoup plus rapide.

Cette agitation augmente avec la température : c’est l’agitation thermique.
- Agitation moléculaire
- Quel que soit leur état, les molécules s’agitent de manière désordonnée. Ce que nous percevons comme la température est une agitation moléculaire. Plus la température est élevée, plus les molécules bougent rapidement.
expérience de la goutte d’encre
cristalisoir, eau chaude, eau froide, encre.
3. Interprétation à l’aide du modèle particulaire
activité p86
Exercice 8 p93
a) mélange et dissolution
assets/4_dissolution_pg.mp4

b) changement d’état
assets/lesÉtatsDeLeau.mp4
c) réaction chimique
Lors d’une réaction chimique des molécules disparaissent (les réactifs) et de nouvelles apparaissent (les produits).
Expériences réaction chimiques
*à faire avec les élèves, pas à pas, sauf combustion (à la paillasse).
− portoir
− 2 tube à essai avec solution de sulfate de cuivre
− 1 tube à essai avec solution KMno4 très diluée
- 1 tube à essai avec vinaigre 8°
- coupelle avec du sucre
- coupelle avec du bicarbonate
- spatule
- bouchons
- 1 pipette compte-goutte NaOH à 0.5M
- 1 bécher d’eau
Oxydoréduction
permanganate de potassium à 1 mmol.L−1 (à vu de nez, 0,1 g dans 100 mL)
puis une pointe de spatule de sucre, mélanger.
3 mL d’hydroxyde de sodium à 0,5 mol.L⁻¹
- Ajouter une petite spatule de sucre (poudre dans le bécher) dans la solution de permanganate (liquide violet) ;
- boucher, agiter précautionneusement jusqu’à dissolution complète ;
- ajouter une pipette d’hydroxyde de sodium ;
- observer et décrire.
Est-ce une réaction chimique ? Pourquoi ?
Dilution
dilution d’une solution de sulfate de cuivre
comparaison avec témoin
- Ajouter un peu d’eau dans un des deux tubes contenant du sulfate de cuivre (liquide bleu) ;
- comparer la couleur avec le témoin.
Est-ce une réaction chimique ? Pourquoi ?
Précipitation
sulfate de cuivre à 0,04 mol.L⁻¹ (1 g de CuSo4.5H2O dans 100 mL)
hydroxyde de sodium à 0,5 mol.L⁻¹
- Dans le tube contenant le sulfate de cuivre (liquide bleu), ajouter une pipette d’hydroxyde de sodium ;
- observer et décrire.
Est-ce une réaction chimique ? Pourquoi ?
Combustion
On craque et brûle une allumette
Est-ce une réaction chimique ? Pourquoi ?
Acide-Base
bicarbonate de sodium
vinaigre
- Enlever le bouchon du tube contenant l’acide acétique (liquide transparent) ;
- Ajouter une grosse spatule de d’hydrogénocarbonate en une fois ;
- observer et décrire.
Est-ce une réaction chimique ? Pourquoi ?
Sublimation
assets/sublimation-of-iodine.mp4
Est-ce une réaction chimique ? Pourquoi ?

Ne pas confondre mélange, changement d’état et transformation chimique.
assets/transformations.mp4
4. Conservation de la masse
act transfo chimique et masse (faire l’expérience en classe)

Lors d’une dissolution, un mélange, un changement d’état ou une réaction chimique, la masse se conserve.
| Fiche de mémorisation active | |
|---|---|
| Où trouve-t-on des molécules ? | Dans toute la matière (objets, animaux, gaz, …) |
| Qu’est-ce que l’agitation thermique ? | Le fait que les molécules s’agitent en permanence. Plus la température est rapide, plus elles s’agitent vite. |
| Qu’est-ce qu’une réaction chimique ? | C’est une transformation dans laquelle des espèces apparaissent, et d’autres disparaissent. |
|
Dans une réaction chimique, qu’est-ce qu’un : • réactif • produit |
• Un réactif est une espèce qui se consomme (disparaît) pendant la réaction. • Un produit est un réactif qui apparait au cours de la réaction. |
| Que peut-on dire de la masse lors d’une réaction chimique ? | La masse est conservée (reste identique). |
| Comment représente-t-on les molécules dans le modèle particulaire ? | On les représente par un symbole. |