La matière est composée de molécules, qui sont elles-mêmes des assemblages d’atomes. Il existe plus d’une centaine d’atomes différents.

Un atome a une taille d’environ 10⁻¹⁰ m (un millimètre coupé en 10 millions).
assets/ceramique.mp4
Atomes dans une molécule d’eau :
Un atome est principalement constitué de vide. Au centre de l’atome des protons de charge électrique plus (+) et des neutrons de charge nulle (0) forment un tout petit noyau. Autour de celui-ci se déplacent des électrons de charge électrique moins (−).
Les protons et les neutrons forment la famille des nucléons
Un atome est électriquement neutre ; il doit donc avoir autant de charge plus que de charge moins.

Les atomes et le tableau périodique
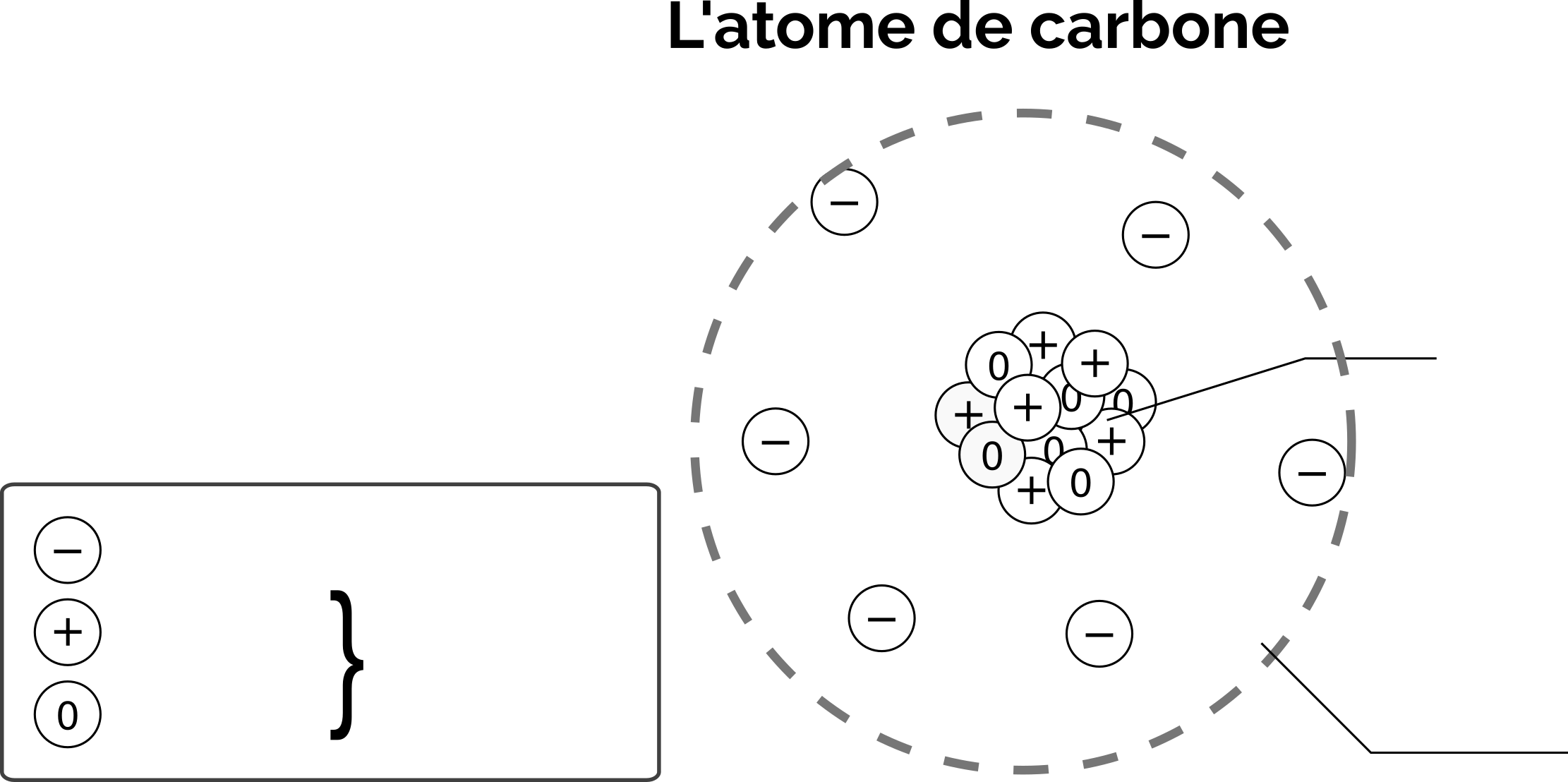
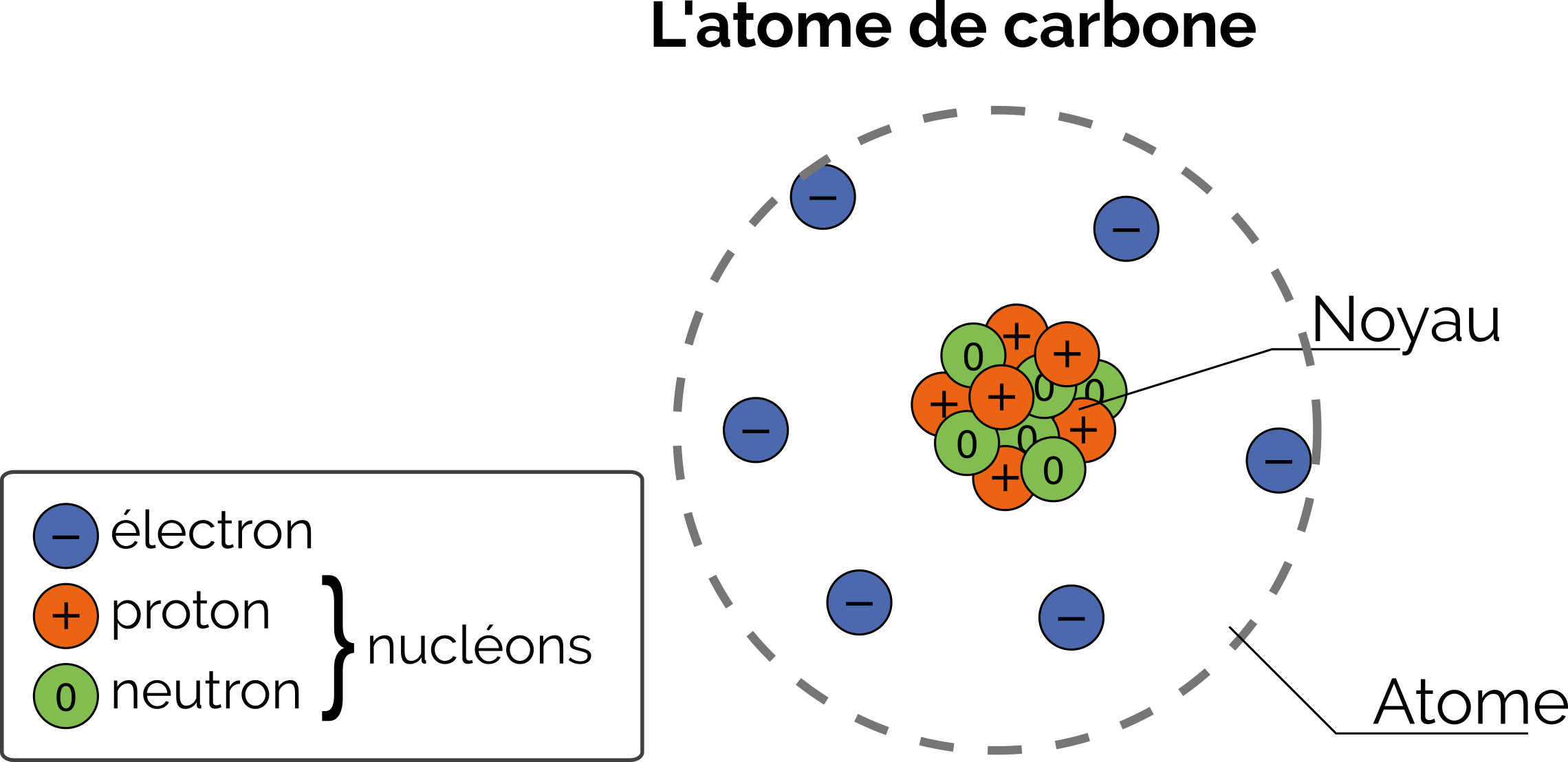
Compléter la représentation de l’atome de carbone avec les mots : atome ; neutrons ; nucléons ; noyau ; protons ; électrons.
Colorier chaque sorte de particule d’une couleur différente.
Représentation de l’atome de carbone (C)

1. Le chlore a pour symbole Cℓ. Il possède 17 protons.
2. C’est le phosphore qui possède 15 électrons et 15 protons.
3. C’est le cuivre de numéro atomique 29.
4. Le fluor.
5. Le krypton possède 36 protons. Son symbole et Kr, il possède 36 électrons.
6.
2,3,5 p 116

Si des électrons ont été perdus, l’ion a une charge positive : c’est un cation. Si des électrons ont été gagnés, l’ion a une charge négative : c’est un anion.
Une solution ionique est toujours neutre. Les charges des cations doivent être compensées par les charges des anions.
Rappel sur la formule chimique
notation
En exposant, on indique la charge électrique dans la formule chimique (par exemple )
Représentation de l’ion Li⁺
Ex p 117 : 9,10,11,12,13,14
Faire quelques expériences de formation de précipité à la caméra. (Fe³⁺)
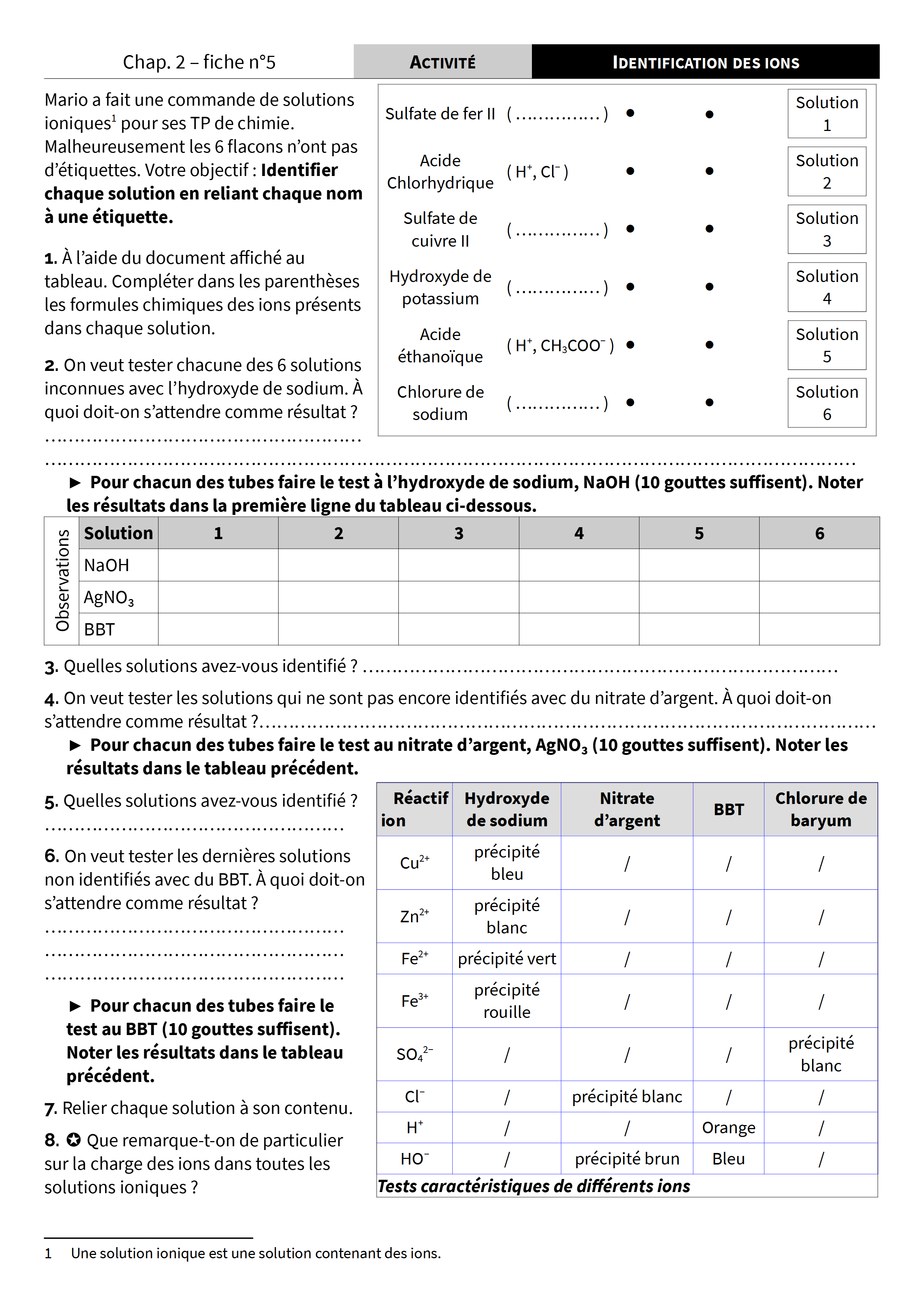
La plupart des ions en solution sont incolores. On peut tout de même en identifier certains grâce à des tests caractéristiques.
Au contact d’un réactif adapté, les ions peuvent former un solide insoluble caractéristique de l’ion. On appelle ce solide un précipité.
paillasse élève :
1 portoir
6 tubes à essais (Vinaigre, FeSO4, Eau salée, KOH, HCl, CuSO4)
NaOH en flacon compte-goutte
paillasse prof :
2 flacons BBT 2 flacons AgNO3
Ex p118 : 17,18,20 +26p118, 30p120
| Fiche de mémorisation active | |
|---|---|
| Quelle est la taille d’un atome ? | |
| Donner les particules qui compose l’atome et leur charge |
proton : charge + neutron : charge nulle électron : charge − |
| De quoi est constitué le noyau de l’atome ? | De protons et de neutrons. On les appele des nucléons. |
| Quelle est la différence entre un atome et un ion ? | Un atome a une charge électrique neutre. Un ion a perdu ou gagné un ou des électrons. Il n’est donc pas neutre. |
| Que symbolisent A,Z et X dans |
A est le nombre de nucléons Z le nombre de protons X le symbole de l’atome |
|
Qu’est ce qu’un cation ? Qu’est ce qu’un anion ? |
Un cation a perdu un électron, il a donc une charge + : Un anion a gagné un électron, il a donc une charge − : |
| Qu’est ce qu’un test caractéristique d’un ion ? | C’est une réaction qui va se produire avec un ion particulier. Si on observe cette réaction, cela veut dire que l’ion était présent. |