Qu’est-ce que le pH ?|une mesure de l’acidité d’une solution
Avec quoi mesure-t-on le pH ?|avec du papier pH, ou un pHmètre
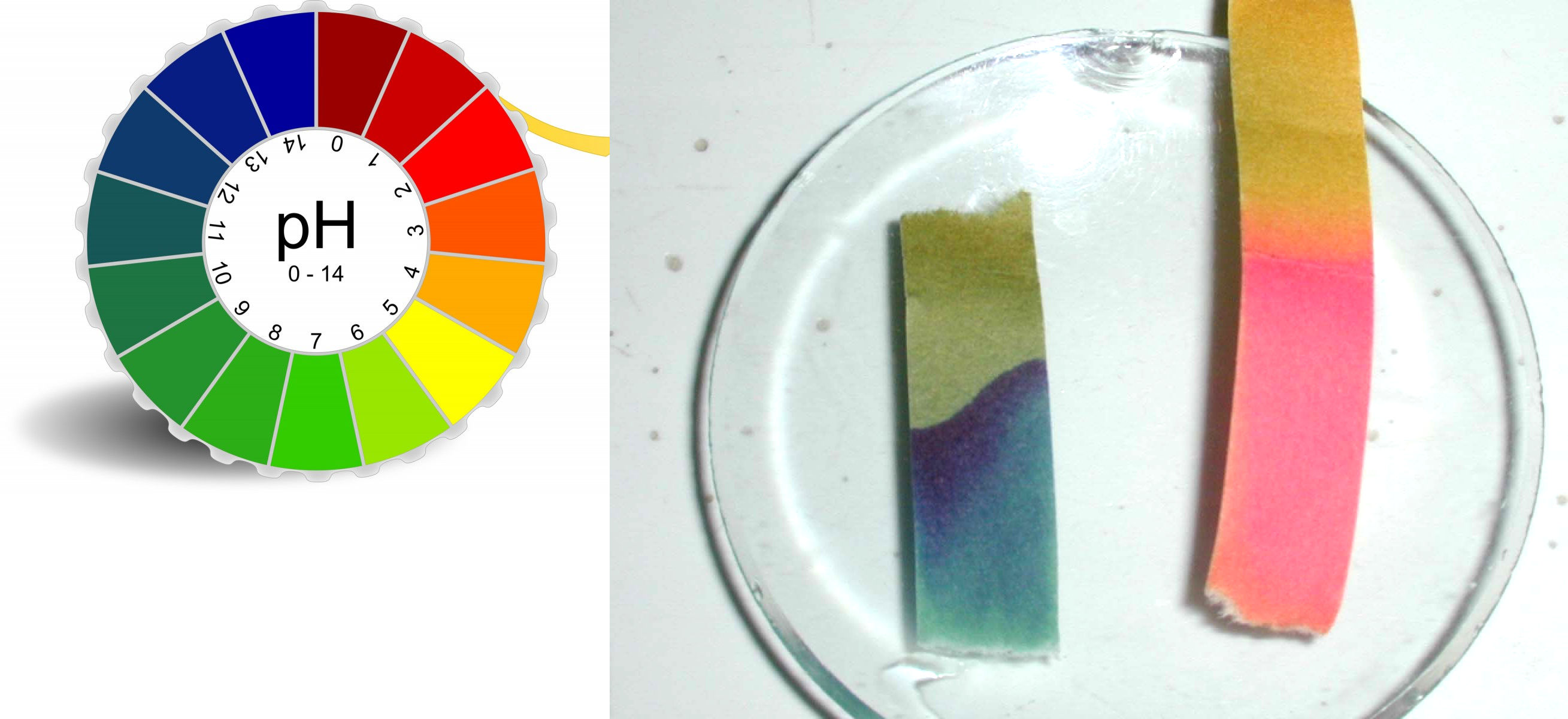
Le pH d’une solution aqueuse est compris entre 0 et 14 :
L’ion H⁺ s’appelle l’ion hydrogène.
L’ion HO⁻ s’appelle l’ion hydroxyde.
Qu’est-ce qu’une solution acide ?|une
solution dont le pH est inférieur à 7.
Elle contient plus
d’ions H⁺ que d’ions HO⁻
Qu’est-ce qu’une solution basique ?|une
solution dont le pH est supérieur à 7.
Elle contient plus
d’ions HO⁻ que d’ions H⁺
Qu’est-ce qu’une solution neutre ?|une
solution dont le pH est environ égal à 7.
Elle contient
environ autant d’ions H⁺ que d’ions HO⁻
Comment s’appelle l’ion H⁺ ? l’ion
HO⁻ ?|l’ion H⁺ est l’ion hydrogène,
l’ion HO⁻ est l’ion
hydroxyde.




Les solutions très acides ou très basiques sont corrosives. Elles peuvent ronger les matériaux et les mains. Il faut donc porter des gants et des lunettes pour les manipuler.
assets/CQFDPeut-on dissoudre un corps dans l’acide.mp4 “Dissoudre un corps dans l’acide ?”
ex 2, 7, 4 p128
Lorsqu’on mélange une solution acide avec une solution basique, les ions réagissent avec les ions selon l’équation :
Les ions et se neutralisent et forment de l’eau.
Comment évolue l’acidité d’une solution acide lorsqu’on lui rajoute de l’eau ?
Comment évolue l’acidité d’une solution acide lorsqu’on la mélange à une solution basique ?
Que se passe-t-il lorsqu’on mélange une base et un acide ?|les ion H⁺ de l’acide et HO⁻ de la base réagissent pour former de l’eau (H₂O)
Dans une réaction chimique qu’est ce
qu’un produit ? un réactif ?|Les réactifs sont les substances
qui réagissent.
Les produits sont les substances qui sont
formées.
Bien expliquer que diluer ≠ concentrer.
CH3COOH à 0,06 M (dilution 20× du vinaigre à 8°) NaOH à 0,5 M
flacon compte-gouttes (soude) ×6 bécher 100 mL (acide) ×6 bécher 250 mL (eau) ×12 ph-mètre ×6 éprouvette 100 mL ×6
au tableau : pH solution acide , pH acide dilué, pH acide+base, pH base dilué

| groupe | pH solution acide | pH acide dilué | pH acide+base | pH base dilué |
|---|---|---|---|---|
| 1 | ||||
| 2 | ||||
| 3 | ||||
| 4 | ||||
| 5 | ||||
| 6 | ||||
| 7 |
Que se passe-t-il lorsqu’on dillue une solution acide ou basique ?|Le pH se rapproche de 7.
ex 10,11,12,13 p129
Souffler dans du BBT ou jus de choux rouge.
Lorsque le dioxyde de carbone (CO₂) se dissout dans l’eau, cela l’acidifie. Les émissions humaines de CO₂ contribue à l’acidification des océans mettant en péril les coraux et l’écosystème marin.
expérience paille de fer + hcl + flamme = bouuum, Al et Zn aussi + test ion
Qu’est devenu le métal ? Serait-il un ion ? Comment le prouver ? +test d’identif.
De nombreux métaux réagissent avec les acides en formant du dihydrogène () et un cation métallique.


assets/combustion-du-dihydrogene-et-du-dioxygene.mp4
Pour le fer, la réaction s’écrit :
indiquer réactifs / produits + état physique
20,22 p 131-132 17 p 130